ایزوتوپ ها چگونه کشف شدند؟
104 سال پیش، روز چهارم دسامبر 1913 (13 آذر 1292)، مقاله ای در مجله مشهور نیچر منتشر شد که یکی از مهم ترین کشفیات تاریخ بشر را مستند کرد. انتشار این مقاله نقطه اوج چندین سال آزمایش بود و قرار بود انقلابی در نحوه درک ما از جهان به وجود آورد.
در دنیای امروز، ایزوتوپ ها نقشی انکارناپذیر در زندگی ما دارند و در هر چیزی که فکرش را بکنید، از درمان سرطان گرفته تا شناساگرهای دود و بمب های اتمی استفاده می شوند. اما تا آغاز قرن بیستم طول کشید تا پرده از راز این همزادهای عنصری برداشته شود.
در این مقاله شما می توانید با دانشمندان پیشرو و یافته های آنها آشنا شوید.
اولین بار، فیلسوف یونانی دموکریتوس یا ذیمقراطیس (Democritus) بود که نظریه اتمی عالم را پیشنهاد داد. طبق نظریه او، اجسام تنها از نظر شکل، موقعیت و چیدمان اتم هایشان با هم متفاوت بودند. برای مثال، اتم های مایعات نرم و گرد بودند؛ در حالی که اتم های جامدات دندانه دار بودند و در نتیجه می توانستند در هم گیر کنند و خیلی سفت یکدیگر را نگاه دارند. دموکریتوس به این دلیل واژه اتم را که در زبان یونانی به معنای تقسیم ناپذیر است، انتخاب کرد که در نظریه او، اتم ها قابل تجزیه نبودند. دو هزار سال طول کشید تا گسترش های بعدی در نظریه اتمی او انجام شود.
پا در هوا!
سال 1789 میلادی، شیمیدان فرانسوی آنتوان لاوازیه (Antoine Lavoisier) وجود 92 نوع مختلف ماده را فهرست کرد. اینها «عناصر» بودند، آجرهای سازنده ای که هر چیزی را در عالم می ساختند؛ اما مشکل اینجا بود که چطور باید آنها را تعریف و طبقه بندی می کردند. به عبارت دیگر، چه خصوصیات مشترکی بین آنها وجود داشت که امکان مرتب سازی آنها را فراهم می کردند؟ شاید اگر لاوازیه زنده مانده بود، خودش این مشکل را حل می کرد؛ اما متاسفانه این دانشمند بزرگ در سال 1794، طی انقلاب فرانسه گردن زده شد. این رخداد سبب شد چالش مرتب سازی عناصر بر دوش دانشمند انگلیسی، جان دالتون (John Dalton) بیفتند.
دالتون به ماهیت گازها علاقه داشت. تا سال 1803، مشخص شده بود بخار آب به شکل گازی مستقل در هوا وجود دارد. دالتون در شگفت بود چطور هوا و آب می توانند همزمان فضای واحدی را اشغال کنند، او استدلال کرد اگر هر کدام از این دو از ذرات مجزایی ساخته شده باشند (که امروزه آنها را به شکل اتم در نظر می گیریم)، شاید بتوان فرآیند تبخیر را به شکل قرار گرفتن مخلوطی از ذرات آب در بین ذرات هوا در نظر گرفت. مجموعه آزمایش هایی که دالتون روی مخلوط گازهای مختلف انجام داد تا این ایده را اثبات کند، منجر به تعیین عدد و وزن تمام ذرات بنیادین شیمیایی شد.
اینکه دالتون دقیقاً چطور به ایده مذکور رسید، در هاله ای از ابهام مانده است؛ اما پاراگرافی که به مقاله منتشر شده در سال 1803 اضافه شد، این چنین توضیح می دهد: «تحقیق درباره وزن نسبی ذرات نهایی اجسام مختلف، موضوعی (تا جایی که من اطلاع دارم) کاملاً جدید است. اخیراً من توانسته ام این تحقیق را با موفقیت چشمگیری انجام دهم.» کارهای دالتون با ارائه نخستین جدول ابتدایی وزن عناصر دنبال شد.
نظریه اتمی دالتون نه تنها نشان داد هر عنصر بر اساس مشخصه وزن اتم های سازنده آن تمیز داده می شود، بلکه همچنین نشان داد تمام مواد از اتم ها ساخته شده اند، تمام اتم های یک عنصر همسان هستند و عناصر مختلف اتم های متفاوتی دارند. با وجود این، او هم گمان می کرد اتم ها قابل خلق یا نابودی نیستند؛ ایده ای که تا حدود 100 سال بعد هم کسی آن را به چالش نکشید.
پرتوهای مرموز
سال 1895، فیزیکدان آلمانی ویلهلم رونتگن (Wilhelm Rontgen)، منبع انرژی مرموزی را مشاهده کرد که به شکل پرتوی نامرئی از یک لامپ کروکس (Crookes Tube) منتشر می شد. وقتی رونتگن دست همسرش را روی صفحه عکاسی و در مسیر این پرتوها قرار داد، توانست عکس حیرت آوری تهیه کند که استخوان های دست همسرش را نشان می داد که در هاله ای از گوشت احاطه شده بود. این تصویر خارق العاده نخستین عکس پرتو ایکس جهان بود. سال بعد فیزیکدانی فرانسوی به نام هانری بکرل (Henry Becquerel) به این موضوع که آیا ارتباطی بین این پرتوهای ایکس تازه کشف شده و دلیل درخشندگی اورانیوم در تاریکی وجود دارد؟، علاقه مند شد. او تکه ای اورانیوم را همراه با یک صفحه عکاسی که در کاغذ سیاه پوشیده شده بود، داخل کشوی میز گذاشت. پس از برداشتن روکش کاغذی، بکرل مشاهده کرد صفحه عکاسی سیاه شده است که نشان می داد اورانیوم هم پرتوهایی نامرئی منتشر می کند.
کشف بکرل در ابتدا توجهات زیادی را به خود جلب نکرد و در سایه کاربردهای پزشکی پرتو ایکس رونتگن قرار گرفت. اما همزمان، یک زوج تازه ازدواج کرده که اتفاقاً هر دو هم فیزیکدان و در پاریس مشغول کار بودند: «پی یر و ماری کوری». پس از تولد اولین فرزندشان در سال 1897، ماری کوری تصمیم گرفت تحقیقاتی نظام مند و اصولی درباره پرتوهای اورانیومی بکرل انجام دهد. پیشرفت به سرعت حاصل شد. طی چند روز ماری کشف کرد یک عنصر دیگر به نام توریم هم همان پرتوهای اورانیوم را منتشر می کند. ماری نتیجه گرفت پرتوهای منتشر شده اورانیوم و توریم حاصل واکنش شیمیایی نیستند، بلکه مستقیماً از خود عنصر سرچشمه می گیرند. او این پدیده را «پرتوزایی» نامید.
اواخر همان سال، سرانجام اتم جایگاهش را به عنوان ذره ای بنیادین که قابل تقسیم شدن نیست از دست داد؛ وقتی جیمز جوزف تامسون (Joseph John Thomson) در آزمایشگاه کاوندیش دانشگاه کمبریج موفق به کشف الکترون شد. زیر دست تامسون، جوانی نیوزلندی به نام ارنست رادرفورد (Ernest Rutherford) کار می کرد؛ فیزیکدانی که یک سال بعد و زمانی که تنها 27 سال داشت، به درجه استادی فیزیک دانشگاه مک گیل مونترال کانادا منصوب شد.
در دانشگاه مک گیل، رادرفورد کارهایش را در زمینه مواد پرتوزا پیگیری کرد. او اثبات کرد چندین نوع مختلف پرتوزایی وجود دارد که هر کدام ذرات متفاوتی منتشر می کنند؛ ذرات آلفا، ذرات بتا و پرتوهای گاما. به عنوان بخشی از این کار، ماهیت شیمیایی فرآیندهای پرتوزایی هم باید مورد بررسی قرار می گرفت. به همین دلیل، رادرفورد به دنبال شیمیدان ماهری بود تا با او همکاری کند. در جستجوی این شخص، رادرفورد به فردریک سودی (Frederick Soddy) رسید؛ دستیار جوانی که در آزمایشگاه های شیمی مک گیل کار می کرد.
همکاری پیشگامانه
همکاری رادرفورد و سودی به خوبی پیش می رفت و آنها در سال 1902، جامعه علمی را با اعلام خبری خارق العاده در بهت و حیرت فرو بردند: «عناصر می توانند به یکدیگر تبدیل شوند.» باور نکردنی بود؛ اما ظاهراً در فرآیند انتشار پرتوهای مرموز، انواع کاملاً جدیدی از ماده خلق می شد که مشخصات شیمیایی و فیزیکی آنها کاملاً متمایز از اتم والد بود. رادیم به رادون تبدیل می شد و یک جامد به شکل گاز در می آمد.
ناگهان پرتوزایی نقل محافل شد و نظریه «واپاشی» رادرفورد و سودی درباره تفکیک اتم ها نه تنها توجه دانشمندان، بلکه نظر عموم مردم را هم به خود جلب کرد. روزنامه نگاران آزمایشگاه رادرفورد را محاصره کردند و پزشکان درباره «آزمایش استنشاق گاز رادیم برای درمان مرض سل» و «اثرات دلچسب ناشی از نزدیک کردن رادیم به چشم» به او نامه نوشتند.
به دنبال موفقیت آنها، در مارس 1903 (فروردین 1282)، سودی برای پیوستن به ویلیام رمزی (William Ramsay) در کالج دانشگاهی لندن برگزیده شد تا به آزمایش محصولات گازی شکل ناشی از واپاشی عناصر بپردازد. وقتی رادرفورد در تابستان آن سال به انگلستان سفر کرد، آنها موفق شدند با همکاری یکدیگر نشان دهند در زنجیره واپاشی که با یک اتم والد ناپایدار اورانیوم آغاز می شود، یک اتم دختر رادیم تولید و یک اتم هلیم آزاد می شود. اتم ناپایدار رادیم هم به نوبه خود به محصول دختر خودش، رادون، واپاشیده می شد و آن هم یک اتم هلیم را آزاد می کرد. این فرآیند همچنان ادامه پیدا می کرد تا در نهایت هشت اتم هلیم آزاد می شدند و یک اتم پایدار کاملاً جدید ظاهر می شد. امروزه می دانیم این عنصر جدید «سرب» بوده است.
پس از یک سال اقامت در لندن، سودی کرسی مدرس شیمی فیزیک و پرتوزایی دانشگاه گلاسکو را پذیرفت؛ جایی که طی 10 سال آینده، به شفاف سازی رابطه بین تعداد فزاینده عناصر پرتوزا و جدول تناوبی کمک کرد. اما طی این دوران، تعدادی از شیمیدانان در آزمایشگاه های مختلف اروپا گزارش کردند چندین عنصر مختلف ظاهر شده اند که اگرچه بطور فیزیکی قابل جداسازی هستند، اما وقتی واکنش های شیمیایی آنها در نظر گرفته می شود، تفکیک ناپذیر هستند. برای مثال، رادیوتوریم که محصول واپاشی توریم بود، از نظر شیمیایی فرقی با توریم نداشت، اما از نظر فیزیکی کاملاً قابل تمیز دادن بود. دانشمندان از خود می پرسیدند چه اتفاقی افتاده بود؟ سودی مسئله را مورد بررسی قرار داد و او هم دریافت جداسازی توریم – 10 از مزوتوریم و رادیم غیر ممکن است و نتیجه گیری کرد این سه عنصر از نظر شیمیایی «همسان» هستند.
راهنمایی: رادیوتوریم و توریم – 10 هر دو اصطلاحاتی متعلق به تاریخ هستند. امروزه آنها را با نام توریم – 228 و رادیم – 224 می شناسیم. مزوتوریم هم در دو وضعیت I و II ظاهر می شد که امروزه رادیم – 228 و آکتینیم – 228 خوانده می شود.
عناصر همسان؟
سال 1911، سودی این مشکل را با قانون «جابجایی عمومی» خود رفع کرد. طبق این قانون، وقتی یک ذره آلفا در واپاشی پرتوزا آزاد می شود، عنصر پرتوزا به اندازه دو جایگاه در جدول تناوبی و در جهت کاهش جرم جابجا می شود. متعاقب آن، وقتی این عنصر تازه دو ذره بتا از دست می داد، به جایگاه اصلی اش باز می گشت. وقتی عنصر به جایگاهش در جدول تناوبی باز می گشت، به همان عنصر اولیه تبدیل می شد، اما وزن آن متفاوت بود. این مسئله توضیح می داد چرا عناصر دختر را نمی توان به روش شیمیایی از عناصر والدشان جدا کرد، اما می توان بر اساس اختلاف وزن شان آنها را تشخیص داد و مطالعاتی که سال بعد بوسیله سودی با دستیارش الکساندر فلک (Alexander Fleck) انجام شد، تایید کرد اثرات مشابهی در بسیاری دیگر از محصولات واپاشی یافت می شود.
در مراسم شامی که پدر خوانده سودی (که او هم شیمیدان صنعتی بود) برگزار کرده بود، بحث درباره این مفهوم جدید مطرح شد و همین جا بود که از سوی یک دوست خانوادگی، دکتر مارگارت تاد (Margaret Todd) نام «ایزوتوپ» برای اتم هایی که از نظر شیمیایی همسان بودند اما وزن متفاوتی داشتند، پیشنهاد شد (واژه ایزوتوپ از کلمه یونانی isostopos به معنای «هم جا» گرفته شده است). سودی اصطلاح ایزوتوپ یا عناصر ایزوتوپیک را اولین بار و در مقاله ای با عنوان Intra-atomic Charge به کار برد که در تاریخ چهارم دسامبر 1913 (13 آذر 1292) در مجله نیچر به چاپ رسید.
با خواندن مقاله سودی، فرانسیس آستون (Francis Aston) فیزیکدان به این فکر افتاد که شاید ایزوتوپ های عناصر دیگر هم وجود داشته باشند، اما وقوع جنگ جهانی اول او را از آزمودن فرضیه اش بازداشت. با بازگشت به کمبریج در سال 1919، او ابزاری را اختراع کرد که امروزه با نام طیف نگار جرمی شناخته می شود؛ دستگاهی که اجزای شیمیایی سازنده یک نمونه را به شکل خطوط متمایز نشان می دهد. آستون نشان داد نئون دو خط طیفی مختلف در وزن های 20 و 22 ایجاد می کند که ثابت می کرد این عنصر دارای دو ایزوتوپ است.
راهنمایی: طیف نگار جرمی ابزاری است که برای تعیین جرم اتم ها استفاده می شود. در این ابزار، باریکه ای از ذرات باردار از میدانی الکترومغناطیسی عبور داده می شود و ذرات با وزن های مختلف جدا می شوند. طیف حاصل روی صفحه عکاسی ثبت می شود.
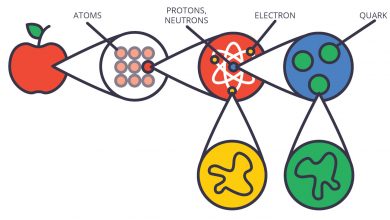
در زمان کشف سودی، هسته اتم به تازگی کشف شده بود و دانشمندان هنوز نمی دانستند هسته اتم خود از دو نوع ذره مختلف ساخته شده است: پروتون و نوترون. امروزه می دانیم موقعیت یک عنصر در جدول تناوبی نه تنها با وزن اتمی، بلکه با عدد اتمی (تعداد پروتون های هسته) آن تعیین می شود.
سال 1921، فردریک سودی جایزه نوبل شیمی را برد. یکسال بعد، این جایزه برای کشف ایزوتوپ های عناصر غیر پرتوزا به فرانسیس آستون داده شد.
کشف ایزوتوپ ها، انقلابی در دانش بشر ایجاد کرد. در پزشکی، ایزوتوپ ها در تصویربرداری استخوان و به عنوان ردیاب برای تشخیص تومورها و لخته های خونی استفاده می شوند. پرتوهای گامای کبالت – 60 در پرتو درمانی (رادیوتراپی) و برای کشتن یاخته های سرطانی استفاده می شوند. در باستان شناسی، کربن – 14 برای تعیین سن نمونه ها استفاده می شود و زمین شناسان از ایزوتوپ های اورانیوم و سرب برای تعیین عمر صخره ها بهره می برند. ایزوتوپ ها همچنین در ساخت حسگرهای دود استفاده می شوند، اما شاید مشهورترین آنها ایزوتوپ اورانیوم – 235 باشد که در ساخت سلاح های هسته ای استفاده می شود.
منابع
مقاله علمی و آموزشی «ایزوتوپ ها چگونه کشف شدند؟»، نتیجه ی تحقیق و پژوهش، گردآوری، ترجمه و نگارش هیئت تحریریه پورتال یو سی (شما می توانید) می باشد. در این راستا مقاله محمود حاج زمان در مجله دانستنیها، به عنوان منبع اصلی مورد استفاده قرار گرفته است.