با اسیدها و بازها آشنا شویم
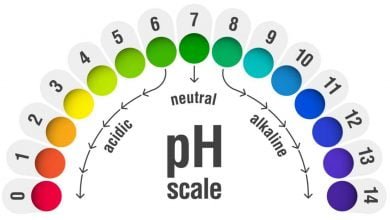
بعضی مواد وقتی با اسیدها و بازها تماس پیدا میکنند، تغییر رنگ میدهند. این مواد را معرّف یا شناساگر مینامند. تورنسل در محلول اسیدی از آبی به قرمز تغییر رنگ میدهد و در محلول قلیایی، از قرمز به آبی میگراید.
بیشتر اسیدها مزه ترش دارند. بعضی اسیدها سمی هستند، بعضی باعث سوختگیهای شَدید میشوند و تعدادی نیز کاملاً بیضرر بهشمار میآیند. بعضی اسیدها نیز خوراکی و بسیار مفید هستند. ما اسید سیتریک را از پرتقال و لیموترش بدست میآوریم. بدنمان هم اسیدهایی را میسازد که به گوارش غذا کمک میکنند.
اسید سولفوریک یکی از قویترین و مهمترین اسیدها است که به مقدار فراوان در تولید انواع کود، فرآوردههای نفتی، آهن و فولاد بکار گرفته میشود. آب باتری اتومبیلها، اسید سولفوریک رقیق شده با آب خالص است. سایر اسیدهای قوی عبارتند از اسید نیتریک و اسید کلریدریک.
بازها یا قلیاها موادی هستند که مخالف و ضد اسیدها بهشمار میآیند. گرچه بعضی بازها از قبیل آهک (هیدروکسید کلسیم) و سود سوزآور، همانند اسیدها، خیلی فعال و خورنده هستند. از بازها در فرآیندهای صنعتی استفاده میشود. هیدروکسید منیزیم (مایع یا پودر سفیدی که برای برطرف کردن درد ناشی از حالت اسیدی معده مصرف میکنیم)، نمونهای از یک باز ملایم است. بازی که در آب قابل حل باشد، قلیا نامیده میشود.
وقتی یک اسید و یک باز به نسبت مناسب با هم مخلوط میشوند، یکدیگر را خنثی میکنند. برای مثال، اگر اسید کلریدریک با سود سوزآور مخلوط شود، حاصل واکنش آنها، نمک معمولی و آب خواهد بود.
منابع
- کتاب Kingfisher Science Encyclopedia. تالیف Catherine Headlam. ترجمه محمود سالک. نشر Kingfisher Books. سال 1991.